リチウムイオン電池とは
1.リチウムイオン電池とは
リチウムイオン電池は、ノーベル賞を受賞された吉野彰先生達により1985年頃に開発され、1990年代に携帯電話や小型ビデオ、ノート型パソコンの電源として商品化が進んだ。また、カリフォルニア州ゼロエミッション構想が同じ頃に発表され、燃料電池自動車(FC-EV)や電気自動車(B-EV)の開発がスタートするとともに、搭載する大容量のリチウムイオン電池の開発が始まる。1)
2.リチウムイオン電池の誕生
初めに充電の出来ない1次電池のリチウム金属電池について記述する。1960年代に米国NASAが高エネルギー密度の電源を必要としたことから電池の研究開発がスタートした。そして宇宙用や軍事用途の電池として米国で開発され、1970年代には民生用のリチウム金属電池が日本で開発され、気象観測用やカメラ用、メモリバックアップ用として広がった。このリチウム金属電池は、正極材料にフッ化黒鉛や二酸化マンガンが使用され、負極材料にリチウム金属が使用された。2)
1次電池のリチウム金属電池を充電可能な2次電池への応用が多くの研究機関で行われたが、負極のリチウム金属部分にデンドライトと呼ばれる針状結晶が生成し、セパレータを突き破り正極側と短絡して発火・破裂事故が多く発生した。この解決策として吉野彰先生達は負極にカーボン材料を使い、正極と負極の間をリチウムイオンがキャッチボール出来るようにした。これが充放電可能な2次電池のリチウムイオン電池である。
近年、樹脂製のセパレータをセラミックス系の全固体型電解質にすることで、負極にリチウム金属を使用してもデンドライト生成による正極側との短絡が発生しないと言われ、全固体電池の開発が進んでいる。リチウム金属を使用することで高エネルギー密度の電池が期待されているが、電気自動車に大量のリチウム金属を搭載するの事は、消防法の面から難しく、水をかけて激しく反応する材料に疑問を持つ研究者は多い。
3.リチウムイオン電池の特長
リチウムイオン電池は、セルあたり3.7Vと他の電池に比べて高電圧である。Ni-MH電池は1.2V、鉛電池は、2.0Vである。また、高エネルギー密度で小型・軽量が可能である。リチウムイオン電池の重量エネルギー密度は、100Wh/kg以上であり、鉛電池の3倍以上、Ni-MH電池の2倍以上の数値となる。自己放電が少なく、Ni-MH電池やNi-Cd電池のようなメモリー効果がない。さらに、長寿命で高信頼性である、などの特長がある。
一方、充放電効率が非常に高いため、過充電による余分なエネルギーは電解液の分解(ガス化)を招き、セルの発熱、さらには発火・破裂の危険となるので、セル電圧の管理を厳密に行う必要がある。3)
4.色々なリチウムイオン電池
正極材料の違いで分類すると、Co系と呼ばれるリチウムイオン電池が最初に登場し、携帯電話やノートパソコンに使用された。次にMn系と呼ばれる電池が開発され、初期の電気自動車に搭載された。高価なCo系を使用しないMn系は、低コストで高い安全性から大容量の電池に良いとされた。しかし、高温環境下でのサイクル試験での特性劣化が大きく、Co系やMn系の良い点を利用したNCM系(Ni、Co、Mnの略。三元系とも呼ばれる)が登場した。初期は1:1:1の比率が主流であったが、最近はNiを多く含む材料が主流である。リン酸鉄系(Fe系)と呼ばれる電池もあり、公称電圧が3.2Vとやや低くなる。
負極材料の違いで分類すると、大部分がカーボン材料であるが、チタン酸リチウム材料を使用し、公称電圧が2.3Vとさらに低くなるが、LTO系電池として商品化されている。
形状について分類すると、外装材料がアルミラミネートの場合と缶(アルミ製、ステンレス製)に分けられる。缶については、その形状が円筒型と箱型に分けられる。図1に様々な形状のリチウムイオン電池を示す。

電解液で分類すると、大部分がエチレンカーボネートやジエチレンカーボネートによる有機系の液体であるが、過去にはポリマー電解質が開発された。現在は固体型電解質の開発が進行している。また、イオン性液体や半固体材料なども開発されている。
5.充電の方法
正極材料にNCM系、負極材料にカーボン、電解液に有機系を使用した標準的なリチウムイオン電池(15Ah)の単セルの充電方法を図2に示す。充電条件は、電池メーカーの推奨する電流・電圧で充電するのが安全で寿命にも良い。図2の電池は1/3C(C:時間の逆数、1/3Cは3時間で充電できる値で15Ahに対して5Aとなる)充電が標準で、5A-4.20VのCC-CV充電となる。3.50V付近から4.20Vまでは5Aで充電し、電池の電圧が4.20Vに達すると電流が低下する。組電池の場合は、各セルを監視する保護回路(Battery Management System)を取り付けて充電する必要がある。
充電で注意すべき点は、低温下で無理な充電を行わない事である。充電とは負極のカーボン材料の中にLiイオンが充填される現象であるが、低温下で無理な充電を行うと均一な充填が出来ずに、部分的に密な部分と疎な部分ができる。密な部分は微視的に過充電状態となり、金属リチウムの生成につながり、針状結晶のデンドライトに成長する可能性がある。このような状態に大きな衝撃が加わると内部短絡による発火・破裂事故の危険性が高くなるので要注意である。

6.放電の方法
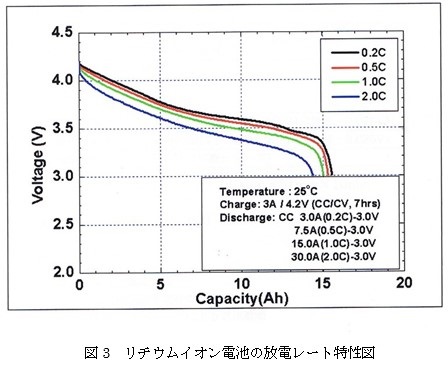
電池メーカーから図3に示すような放電レート特性の図が提供される。この図は、0.2C、0.5C、1.0C、2.0Cの各レートで放電した場合の電池電圧の変化である。横軸に容量(Ah)、縦軸にセルの電圧(V)を示している。この図から読み取れるのは、使用する電流が大きくなると電圧の低下があり、使用できる容量が少なくなる。大きな電流で放電すると、内部抵抗により電池の電圧はさらに低くなり、下限電圧に到達するのも早くなる。このデータを見ながら、使用する電流値と容量(あるいは稼働時間)の計算に役立てる事ができる。
7.輸送時の注意
リチウムイオン電池は、国連の航空危険物規則書(UN規則)に従って輸送する必要がある。宅配便など国内のトラック輸送は該当しないが、航空貨物を利用する場合は、UN規則に従った試験を行い、合格してから航空貨物(危険物として)に搭載できるようになる。4)
参考文献
1) 松尾博「二次電池の材料に関する最新技術開発」第15章第1節 2022年6月 技術情報協会
2) 江田信夫、勝山春海「リチウムイオン電池」電池応用ハンドブック第1-2章 2005年1月 CQ出版社
3) 松尾博「リチウムイオン電池における高容量化・高電圧化技術と安全対策」第13章第5節 2018年10月 技術情報協会
4) 電池工業会「リチウム金属およびリチウムイオン電池の輸送に関する手引書」第4版 2009年4月
(著)マイクロ・ビークル・ラボ株式会社